10. 熱機関の効率とエントロピー
10-1.熱の移動と、エントロピー変化:エントロピー増大則、可逆と不可逆
前回紹介した、熱力学の3法則の式と意味は、
1) \(dU=dQ+dW = dQ-PdV+dW' \)
熱はエネルギーであり、力学的エネルギーと熱エネルギーを加えたものは保存する。
2) \( dS= \sum_i{dS_i}=\sum_i{\frac{dQ_i}{T_i}} \geq 0 \)
熱は低温物体から高温物体へは流れない(氷でお湯を温められない)。これを「エントロピー変化」と言う量を導入して表現すると、「エントロピー変化は現象しない」と言う形にまとめられる。これを「エントロピー増大則」とも言う。
3) \(S(T=0)=0\)
絶対温度0度のエントロピーは0とする。この基準と第2法則の「エントロピー変化」を組み合わせると、任意の状態のエントロピーが定義される。
----
ここまででは、特に「エントロピーって(確かに定義はされているけど)何?」と言うことがわかりませんね(^^; また、「氷でお湯を温められない」と言う、当たり前にも思えることが、何の役に立つ(知見を広げる)の? と思うかもしれませんね。そこでまず、「\( dS \geq 0 \) 」と「氷でお湯を温められない」が、同じ意味である」ことから説明していきます。
今、温度\(T_1\)の物体(1) と温度\(T_2\)の物体(2) があったとします。この2つの物体を接触させ、物体(2) から b物体(1) に、熱\( dQ_{1 \leftarrow 2 } \)が移動したとします。物体(1) が受け取った熱は\( dQ_1=dQ_{1 \leftarrow 2 } \)で、物体(2)が受け取った熱は\( dQ_2= -dQ_{1 \leftarrow 2 } \)となります。この時、熱力学第2法則で定義されているエントロピー変化は、\[dS= \sum_i{dS_i}=\sum_i{\frac{dQ_i}{T_i}} \] \[= \frac{dQ_1}{T_1} + \frac{dQ_2}{T_2}\] \[= \frac{dQ_{ 1 \leftarrow 2 } }{T_1} + \frac{-dQ_{1 \leftarrow 2} }{T_2} \] \[= dQ_{ 1 \leftarrow 2 } \left( \frac{1 }{T_1} - \frac{1 }{T_2} \right)
\] \[= dQ_{ 1 \leftarrow 2 } \frac{T_2-T_1 }{T_1 T_2} \] となります。
ここで、\( dQ_{1 \leftarrow 2 }> 0 \)の場合を考えます。つまり「(2)から(1) に正の熱が移動する」場合、言い換えれば「(2)が(1)を温める」場合を考えます。温度は「絶対温度」で考えますので、常に正の値です。すると右辺は、\(T_2>T_1 \)なら正、 \( T_2 < T_1 \)なら負の値になります。つまり、高温の物体が低温の物体を温めるなら正、低温の物体が高温の物体を温めるなら負の値になります。低温の物体が高温の物体を温めるとはたとえば「氷でお湯を温める」ことで、これは実際には起こりません。つまり、実際に起こる熱移動は、\(dS\)が負にならない、つまり \[dS \geq 0\] と表せます。これが「エントロピー増大則」です。増大則と言いますが、エントロピー変化は負にならなければよいので0でもかまいません。
なお\(\frac{dQ}{T}\)は、その「物体が受け取る熱 / その物体の温度」であり、低温であるほど大きくなる量です。低温であるほど「熱を受け取りやすい」ですので、個々の物体のエントロピーは「その物体の熱の受け取りやすさ=温めやすさ」を表していると思っても良いでしょう。すると「それぞれの物体の温めやすさの和を取ると、それが0または正になる方向にしか熱は移動しない」と言っても良いと思います。そういう「熱の移動方向」を表す法則が、熱力学第2法則(エントロピー増大則)です。
【エントロピー増大則と時間:可逆変化と不可逆変化】
エントロピーは必ず増大する(減少しない)というのが、自然法則であれは、「一旦増えたら、元には戻れない」ということを意味します。エントロピー変化0であれば、元に戻るのも「減少はしない」ですから、「元に戻れる変化は、エントロピー変化=0である」ということになります。元に戻れる変化を「可逆変化」と呼び、元に戻れない変化を「不可逆変化」と呼びます。例えば「氷とお湯を混ぜたら、ぬるま湯になる」という変化は、「ぬるま湯が、氷とお湯になる」ということは起らないので不可逆変化です。このときにはエントロピーは増大しています。一方、「気体をゆっくりと断熱圧縮する」とか「気体をゆっくり等温圧縮する」とかの変化は、エントロピーが増大せず(\(dS=0\))元に戻すことができます。これを「可逆変化」と言います。自然界には「過去から未来への変化は起こる」けど、時間的に逆転した変化(ビデオの逆回し)は、起こることと起こらないことがあります。何故かはわからないけど、それを定式化したのが「熱力学の第2法則(エントロピー増大則)」と位置付けることができます。
なお「殆ど、いつも熱平衡状態にあると近似できるような状況で、ゆっくり変化させる」ことを準静的過程と言います。準静的過程でない場合、つまり「一気に変化させる(例:気体の拡散など)」場合には、エントロピー変化は0(\( dS=0\))ではなく、必ず増えます(\(dS>0\))。つまり、準静的過程でない場合には、必ず不可逆(逆転して現象は起こらない)になります。
10-2. 熱機関。熱機関の熱効率
ではここで、熱エネルギーと力学的エネルギーの変換について、考えてみます。「力学的エネルギー(仕事)を熱エネルギーに変える」ことは、たとえば摩擦を使えばできます。法則として意識されたのは19世紀ですが、「手をこすれば暖かくなる、木をこすれば火を起こせる」等の現象はたぶん有史以前から知られていたと思います。例えば「速さ\(\upsilon\) で運動しているもの(運動エネルギー\( K=\frac{1}{2}m\upsilon^2 \))」が、摩擦で静止すると、(エネルギーが保存すれば)持っていた「運動エネルギー」は全て「熱エネルギー」に変換されます。実際にジュールがこの測定をして、熱がエネルギーの一種であること見出したのですから。
つまり「(力学的)仕事は、全て熱に変換できる」ことが分かります。これを、
「 dW(仕事)→[摩擦]→dQ(熱) 」
と書きましょう。(何を「あたりまえ」のことを... と思いますか?(^^;)それでは逆に、「熱エネルギーを、(力学的)仕事」に変換することは、できるのでしょうか?この問題を考えていきます。
熱を仕事に変換する装置を「熱機関(エンジン)」と呼びます。なお、このような研究が始まった時代はちょうど「蒸気機関(蒸気エンジン)」が発明された時代です。現在では蒸気エンジン以外にもガソリンエンジンやディーゼルエンジン、ジェットエンジンやロケットエンジンもありますが、それらは全て「燃料を燃やして熱を発生させ、その熱(エネルギー)を力学的エネルギー(仕事)に変換して、物を動かす」仕組みです。それらすべてを「熱機関(エンジン)」と呼びます。では、「工夫したエンジンを作れば、熱エネルギー全て仕事に変換すること」ができるのでしょうか?
もし、「熱エネルギーを全て仕事に変換する熱機関」が存在するなら、それを、
「 dQ(熱)→[熱機関]→dW(仕事) 」
と書きましょう。ちょうど「摩擦」の逆です。
ここで、この装置と摩擦を組み合わせた装置を作ってみます。
「 dQ(熱)→[熱機関]→dW(仕事)→[摩擦]→dQ(熱) 」
熱が仕事に変わりそれがまた熱に変わっただけですね...(何が面白いの?と思うかもしれませんね(^^;) ですが... 最初の「熱機関が熱を取り入れる場所」と最後の「摩擦で熱を発生する場所」は、一般には別の場所でも良いはずです。するとこの装置は「熱を別の場所に運ぶ装置」になります。そして... この話には「どこにも温度の話が出てきていない」ことに注目してください。つまり温度とは無関係に「熱を運ぶ装置」になります。これを使えば例えば「氷(低温物体)の熱で熱機関を動かし、その動力(仕事)を使って、お湯(高温物体)の中で摩擦を起こして熱を発生させ、お湯を温める」つまり「氷でお湯を温める装置」になりますヽ(^o^)丿
こんな装置、あったら便利ですね。キャンプでも災害時でも、そこからの水取ってきてこの装置を使えば、どんどん熱を移動して「氷とお湯」が(他の燃料や動力無しで)できあがります。
でも「氷でお湯を温める」装置は誰も作ることができないばかりか、そのような現象を見た人すら、誰もいません。それが熱力学第2法則です。つまり、「熱を全て仕事に変える装置は存在しない」と結論できます。
もちろん、全て変えることが出来なくても「熱を(一部分)仕事に変える装置」は存在します。ではどのくらい仕事に変えることが出来るのでしょうか? 熱機関が、\(dQ_1\)の熱をもらって\(dW\)の仕事(力学的エネルギー)に変換したとき、\( \frac{dW}{dQ_1}\) つまり貰った熱と発生した仕事の割合を「熱効率」と呼び \( \eta \)(ギリシャ文字のイータ)と書くことにします。\[ \eta= \frac{dW}{dQ_1} \] まったく動かない(仕事を取り出せない)熱機関は熱効率0です。なおこの量を使うとさっきの話は「熱効率\(
\eta=100\% \)の熱機関は存在しない」と言うこともできます。なら「最大の熱効率は、いくつまで可能」なのでしょうか? 歴史的には、この問題を最初に解いたのがカルノーで、それを元にして複雑な計算を経てエントロピーの概念や熱力学の3法則が発見されたのですが、ここでは「熱力学の3法則に基づき」熱機関の最大熱効率を求めてみましょう。
まず、熱機関を
「 dQ1(熱)→[熱機関]→dW(仕事) 」
と表します。貰った熱を\(dQ_1\) 熱機関から取り出す(力学的)仕事を\(dW\)とします。
熱効率は、\[ \eta= \frac{dW}{dQ_1} \]
です。
 ところで、熱力学の第一法則(エネルギー保存則)から、「もらったエネルギーは出ていくエネルギーと等しい」という関係になります。今の場合、貰った熱(エネルギー)と出ていく仕事(エネルギー)の量が違うわけですから、残りのエネルギーがあります。これは「熱」\(
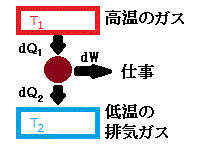
dQ_2\)として排出されます。一般にエンジンは、燃料を燃やして「高温のガス(温度 \( T_1 \) )」を作り、高温のガスから熱エネルギー \( dQ_1\) をもらい、熱機関(エンジン)で(力学的)仕事 \( dW \) を取り出し、残りのエネルギーを低温(温度 \(T_2 \) )の排気ガスの熱 ( \( dQ_2 \) ) として、外界に放出します(右図)。
ところで、熱力学の第一法則(エネルギー保存則)から、「もらったエネルギーは出ていくエネルギーと等しい」という関係になります。今の場合、貰った熱(エネルギー)と出ていく仕事(エネルギー)の量が違うわけですから、残りのエネルギーがあります。これは「熱」\(
dQ_2\)として排出されます。一般にエンジンは、燃料を燃やして「高温のガス(温度 \( T_1 \) )」を作り、高温のガスから熱エネルギー \( dQ_1\) をもらい、熱機関(エンジン)で(力学的)仕事 \( dW \) を取り出し、残りのエネルギーを低温(温度 \(T_2 \) )の排気ガスの熱 ( \( dQ_2 \) ) として、外界に放出します(右図)。
熱力学の第一法則(エネルギー保存則)より、「もらったエネルギーは、出ていくエネルギーに等しい」ので、\[ dQ_1= dW + dQ_2\]となります。
また、\( dQ_1 \) は高温のガスが熱機関に「与えた」熱量だから、高温のガスが「もらった」熱量は\( -dQ_1 \) になることに注意すると、エントロピー変化は、
\[ dS= \frac{-dQ_1}{T_1} + \frac{dQ_2}{T_2}\]
なので、熱力学第2法則(エントロピー増大則 \( dS \geq 0\))より
\[ \frac{-dQ_1}{T_1} + \frac{dQ_2}{T_2} \geq 0\]
ここで、\( dQ_1= dW + dQ_2\) , つまり \( dQ_2= dQ_1 -dW \)なのでこれを代入すると、
\[ \frac{-dQ_1}{T_1} + \frac{dQ_1 -dW }{T_2} \geq 0\]
となります。この式には、\( dQ_1, dW, \)と温度しか含まれていないので、この式を変形して\(\frac{ dW}{dQ1}\)を求めます。
\[ \frac{-dQ_1}{T_1} + \frac{dQ_1}{T_2} - \frac{dW }{T_2} \geq 0\] \[ dQ_1 ( -\frac{1}{T_1} + \frac{1}{T_2} ) - \frac{dW }{T_2} \geq 0\] \[ \frac{dW }{T_2} \leq dQ_1 ( -\frac{1}{T_1} + \frac{1}{T_2}
) \] \[ \frac{dW }{dQ_1} \leq T_2( -\frac{1}{T_1} + \frac{1}{T_2} ) \] \[ \frac{dW }{dQ_1} \leq 1 - \frac{T_2}{T_1} = \frac{T_1-T_2}{T_1} \]
つまり、熱機関の熱効率は、
\[ \eta= \frac{dW}{dQ_1} \leq 1 - \frac{T_2}{T_1} = \frac{T_1-T_2}{T_1} \]
となり、最大でも\( \frac{T_1-T_2}{T_1} \)であることが分かります。なお最大値を取るのは\(dS=0\)のとき、つまり「可逆変化のみで作られた熱機関(可逆機関)」です。
10-3. 温度とは? 熱力学的温度定義
つまり、熱機関の熱効率は、
\[ \eta= \frac{dW}{dQ_1} \leq 1 - \frac{T_2}{T_1} = \frac{T_1-T_2}{T_1} \]
であり、可逆機関であれば、
\[ \eta= \frac{dW}{dQ_1} = 1 - \frac{T_2}{T_1} = \frac{T_1-T_2}{T_1} \]
となります。なお「可逆機関」は作ることが可能で、\( dW, dQ \) は、比較的精密に測定することができます。つまり可逆機関の熱効率は「現代の技術で、高い精度で実際に測定することが可能」な量です。ところで可逆機関の熱効率の式を変形すると、
\[ \eta= 1 - \frac{T_2}{T_1} \]
\[ T_2 = T_1 (1 - \eta ) \]
あるいは、
\[ T_1 = T_2 / (1 - \eta ) \]
となり、可逆機関を動かすときの、一方の熱源の温度を基準として決め、熱効率\(\eta\)を測定すれば、他方の温度が決まる、という式になっています。
つまり「温度基準を1つ決め、熱効率を測定することにより、他方の温度を決める(定義する)」ことができます。これを「熱力学的温度計」と呼び、この熱力学的温度計で測った値を「熱力学的温度」と呼びます。なお2019年までの国際標準単位系(SI)では、水の3重点を273.16K(ケルビン)とする基準で、熱力学的温度計で測った値を「温度」と定義するという方法でした。 なお現在はボルツマン定数の値を固定するという方で、温度を定義しますが、この話は次回行います。
また、完全に可逆機関でなくても、ある程度可逆機関に近い仕組みのエンジンなら(エンジンで物を動かすだけでなく、逆にエンジンに(力学的に)仕事を与えて、エンジンを強制的に動かすことができる仕組みのものなら)、「氷でお湯を温める装置」を作ることができます。
10-4.ヒートポンプ(クーラーやエアコンや冷蔵庫)の原理
前の熱機関(エンジン)の話では、「高温の物体から熱をもらい、仕事を取り出して、残りの熱を低温の物体に放出する」という話でした。この場合は\(T_1>T_2, dW>0\)という条件で\(dS \geq 0\)から熱効率を求めました。
逆に\( dW<0 \)とすると\( dQ_1<0, dQ_2<0 \) となり、これが\(T_1>T_2\)でも起こりうる(\(dS \geq 0\)を満たす)ことを示すことができます。これは「低温の物体から熱をもらい、高温の物体を温める装置」つまり「氷でお湯を温める装置」になります。初めの話を違うのは「仕事を与える」というところです。現実には「冷蔵庫、クーラー(エアコン)」などがこれに当たります。電気でモーターを回し、その仕事で「熱機関」を動かします。その時「低温の物体(冷蔵庫の中、冷えた部屋)から熱をもらい、高温の物体(冷蔵庫の外、熱い室外)に熱を放出する」ことが可能です。
不等式の不等号は、負の数を掛けると逆転しますので、その辺をちょっと注意して、前のエンジンの話(計算)を「置き換えて」いきましょう。
まず、向きが全部逆なので、前に書いた量を全て正負逆転しておきます。
\( dQ_1 \rightarrow -dQ_1, dQ_2 \rightarrow -dQ_2, dW \rightarrow -dW \)
すると、
熱力学の第一法則(エネルギー保存則)は、\( -dQ_1= - dW - dQ_2\)で、これは\( dQ_1= dW + dQ_2\)となり、式は前と同じです(意味は正負逆転しています)。
また、\( dQ_1 \) は高温のガスが熱機関から「もらった」熱量、\( dQ_2 \) のガスが熱機関に「与えた」熱量だから、低温のガス「もらった」熱量は\( -dQ_2 \) になることに注意すると、エントロピー変化は、
\[ dS= \frac{dQ_1}{T_1} + \frac{-dQ_2}{T_2}\]
なので、熱力学第2法則(エントロピー増大則 \( dS \geq 0\))より
\[ \frac{dQ_1}{T_1} + \frac{-dQ_2}{T_2} \geq 0\]
ここで、低温物体(2)から奪う熱量\( dQ_2\)と熱機関に与える仕事\(dW\)の関係を知るために、\( dQ_1= dW + dQ_2\) を代入すると、
\[ \frac{dW + dQ_2}{T_1} + \frac{-dQ_2 }{T_2} \geq 0\]となります。この式には、\( dQ_2, dW, \)と温度しか含まれていないので、この式を変形して\(\frac{ dQ_2}{dW}\)を求めます。
\[ \frac{dW}{T_1} + \frac{dQ_2}{T_1}- \frac{dQ_2}{T_2} \geq 0\]
\[ \frac{dW}{T_1} +dQ_2( \frac{1}{T_1}- \frac{1}{T_2} ) \geq 0\]
\[ \frac{dW}{T_1} +dQ_2 ( \frac{T_2-T_1}{T_1 T_2} \geq 0\]
\[ \frac{dW}{T_1} \geq dQ_2 ( \frac{T_1-T_2}{T_1 T_2} \]
\[ dW \geq dQ_2 \frac{T_1-T_2}{T_2} \]
ここで\(T_1>T_2\)なら\(T_1-T_2>0\)なので、
\[ dW \geq dQ_2 \frac{T_1-T_2}{T_2} \]
\[ dW \frac{T_2}{T_1-T_2} \geq dQ_2 \]
\[ dQ_2 \leq dW \frac{T_2}{T_1-T_2} \]
\[ \frac{dQ_2}{dW} \leq \frac{T_2}{T_1-T_2} \]
となります。
つまり、仕事\(dW>0\)を使い「低温\(T_2\)の室内」から熱\( dQ_2 \) を奪い、高温\(T_1\)の室外に熱を放出することができます。ただしこの式は不等号ですから、等号に近い時(\(dS=0\)に近い時)に\(dQ_2>0\)にすることができます。つまり「可逆機関に近い熱機関」であれば、「氷から熱を奪い、お湯に熱を与える」ことが可能になります。これが「クーラや冷蔵庫」の原理です。なおこの限界は\(T_1\)が小さいほど高くなりますから、「クーラーは室外機を冷やすほど、よく冷える。冷蔵庫は裏の放熱器を冷やすほど、よく冷える」という結果になります。これは生活の知恵(と言うか常識?)としても大切な知識かもしれません。
なお今は「低温物体から熱を奪う」ことに主眼をおきましたが、「高温物体に熱を与える」方に注目すれば「エアコン暖房」の原理になります。なお、計算するまでもなく、\( dQ_1= dW + dQ_2\) ですから、電気エネルギーをそのまま熱に変える「電気ストーブ」よりも、「寒い室外からもらった熱に、熱機関がもらったエネルギーを加えた方が大きい」ので、同じエネルギー(電気量)ならば、エアコン暖房の方が電気ストーブより多く発熱することがわかります。まさに「氷でお湯を温める」効果が加わりますから。
10-5. まとめと予告
「氷でお湯を温められない(何も動力を使わない場合)」と言う「一見当たり前に思えそうなこと」は、実は不思議な現象で、これをエントロピー変化と言う量を使って表すと、エントロピー変化は常に0または正、と定式化できます。これが「熱力学第2法則」で、エントロピー増大則とも呼ばれます。
この法則を認めると、熱機関(エンジン)の熱効率は100%は不可能で、最大熱効率が存在することがもとまります。また、最大熱効率が得られるのは「可逆機関(逆転可能な仕組みだけで作る熱機関)」の場合であり、しかも「可逆機関の熱効率」は細かい仕組みや使っている物質によらず「温度だけ」で決まります。この性質を利用すると「温度計」を作ることができ、これを「熱力学的温度計」と呼びます。つい最近まで(2019年まで)、「温度」とは、この「熱力学的温度計で測った値」と、国際標準単位系(SI)では定められていました(現在の話は次回)。
また、熱力学の第二法則と熱力学の第一法則を組み合わせると、熱機関の熱効率だけでなく、逆の仕組みである「ヒートポンプ(動力を使って、熱を移動させる装置)」の効率なども計算できます。ヒートポンプは「クーラ、冷蔵庫、エアコン」などに使われている「動力を使って熱を移動する装置」で、その熱効率の計算結果から、「クーラーの室外機は涼しいところに置くと良い」とか「冷蔵庫の裏の放熱器は壁から離して、熱が篭らないようにすると良い」とか、そう言う電気製品の効率的な使い方も、知ることができます。
このように「なんとなく」熱について調べられてきましたが、ここまでの話では、そもそも「内部エネルギー」って何なのでしょう? そもそも「エントロピー」って何なのでしょう? と言う問題は何一つ解決していません。また、「なぜエントロピーは増大するの?(減少しないの?)」と言う問題も、また「なぜ、可逆変化と不可逆変化が存在するの?」と言う問題も、何も解決していません... と言うか、(初めは当たり前と思っていたことを)知れば知るほど「疑問」が沢山出てきます。
そのような疑問に対して「物質って.... 本当は小さな粒(粒子・分子)が集まってできているのでは?熱って、沢山の粒子の「運動」なのでは?」と(根拠が何も知られていない19世紀の時代に)思った(妄想?)天才がいます。ボルツマンと言う人です。次回は、ボルツマンが考えた「小さな粒子がものすごく沢山集まって、物質が作られている」と言う視点で、熱現象を理解していきましょう。
# なお、物質が小さな粒子が集まってできていていることが「実証」されたのは20世紀初頭です。
では、今日は、このへんで終わります。
 ところで、熱力学の第一法則(エネルギー保存則)から、「もらったエネルギーは出ていくエネルギーと等しい」という関係になります。今の場合、貰った熱(エネルギー)と出ていく仕事(エネルギー)の量が違うわけですから、残りのエネルギーがあります。これは「熱」\(
dQ_2\)として排出されます。一般にエンジンは、燃料を燃やして「高温のガス(温度 \( T_1 \) )」を作り、高温のガスから熱エネルギー \( dQ_1\) をもらい、熱機関(エンジン)で(力学的)仕事 \( dW \) を取り出し、残りのエネルギーを低温(温度 \(T_2 \) )の排気ガスの熱 ( \( dQ_2 \) ) として、外界に放出します(右図)。
ところで、熱力学の第一法則(エネルギー保存則)から、「もらったエネルギーは出ていくエネルギーと等しい」という関係になります。今の場合、貰った熱(エネルギー)と出ていく仕事(エネルギー)の量が違うわけですから、残りのエネルギーがあります。これは「熱」\(
dQ_2\)として排出されます。一般にエンジンは、燃料を燃やして「高温のガス(温度 \( T_1 \) )」を作り、高温のガスから熱エネルギー \( dQ_1\) をもらい、熱機関(エンジン)で(力学的)仕事 \( dW \) を取り出し、残りのエネルギーを低温(温度 \(T_2 \) )の排気ガスの熱 ( \( dQ_2 \) ) として、外界に放出します(右図)。