例えば鍋に水を入れ、そこに焼いた石を入れると、水の温度が上がりお湯になりますね?(って「石焼き鍋」です(^^;)。この現象を昔の人は、石が持っていた「何か」が水に移動したため、水の温度が上がった、と解釈し、その移動した「何か」を「熱(heat)」と呼びました。最初は、目には見えないけど、何か「物質」のようなイメージで「熱素」とも呼ばれていました。
熱現象について、17世紀の「蒸気機関」の発明以来、熱についての様々な実験的研究が進み、熱についての法則がいくつも分かってきます。19世紀にはそれらが「熱力学」という形でまとめられ、様々な法則は「熱力学の3法則」と呼ばれる基本法則と、物質の性質を記述する「状態方程式」から、導ける形に整理されていきました。
ここではまず最初に、熱現象の基本法則としてまとめられた「熱力学の3法則」から紹介していくことにします。
熱力学の3法則は、Wikipedia https://ja.wikipedia.org/wiki/%E7%86%B1%E5%8A%9B%E5%AD%A6 などにもありますが... 説明が長いですね(^^;; 実は熱力学については「歴史的な論理展開や細かい応用について複雑にたくさん書いてある本」は多いのですが「簡潔にまとめている本」は殆どありませんし、ネットでも簡潔な説明は見当たりません。誰か1人の天才がまとめたというよりは、数人の秀才が似たようなことに部分的に気が付き、それらが次第にまとめられ「熱力学の3法則」と呼ばれるようになったからかもしれません。
そこで、その内容を、(式を使い)簡単にまとめます。
1) \(dU=dQ+dW = dQ-pdV+dW' \)
2) \( dS= \sum_i{dS_i}=\sum_i{\frac{dQ_i}{T_i}} \geq 0 \)
3) \(S(T=0)=0\)
量の定義や式の説明は、これから順にしていきますが、熱に関する「基本法則」は、これだけです。それと、物質の性質を記述する状態方程式がありますが、例えば理想気体という物質なら\(PV=nRT\)で、実際の物質を問題にする場合には、物質に応じて、状態方程式は若干変わります。
例によって「これだけ」なのですが、これだけでは意味がわかりませんね(^^; それより「熱」と言う「言葉の意味」すら、まだ説明していませんね。そこで、法則の前まず「用語の意味」を整理し、その次に、第一法則から順に、説明していきます。
まず「熱」とは何か? 温度が高いお湯に手を入れると「熱い!」と感じ、そのままにしておくと(できれば、ですか)火傷しますよね。漢字が同じなので、なんとなく熱いと同じような感じの意味かな?と思うかもしれませんね(^^; その前に「温度」って何でしょ?(^^; 「小学校で教わっている」と思うかもしれませんが、実は「温度の本当の意味」は、高校までの理科には出てきません(なんか、前回の磁石の極の話のようですね)。結構難しい話なので、多分「次回」温度とは何かを正確に説明することになると思います。でも...温度という量が必要になりますので... 「とりあえず」温度とは温度計で測った値と思ってください。なお小学校~高校の段階でも、温度を「温度計で測った値」と定義してします(^^; このような決め方を一般的に「操作的定義」と呼びますが、これは「温度計はそのような仕組みのもので、どのように作ったものなのか」をきちんと定義しないと、定義にならない、まあ誤魔化しみたいな定義です(^^; なお(次回説明する予定ですが)現在では「熱力学的温度計」という温度計で測った値を「温度」と定義することが普通です。そういう意味では小中学校で教わった温度の定義も、「熱力学的温度計の名前や原理(=温度の本当の定義)を説明をしていないだけで」まあ、誤りではないと言えます。
前置きはこの辺にして... とりあえず「温度は温度計で測った値(温度計の仕組みは後回し)」で話を進めていきます。
「熱い」と感じる物の温度を測ると「温度が高い」く、「冷たい」と感じる物の温度を測ると「温度が低い」ことがわかりますが、実際にいろいろ測ってみると、必ずしも「熱い・冷たいの感覚」と「温度計の値(=温度)」は対応するとは限らない、ということも分かります。例えば「70度のお湯」に手を入れると結構「熱く」感じますし、もし全身を入れると(70度の風呂に入ると)... 我慢して入れれば、ですが、多分全身火傷のような感覚になります。一方、70度のお湯を口に入れると、普通に飲めますし、飲む前に煎茶の葉っぱを浸けておけば「ちょうど飲み頃のお茶(^^)」になります。また、気温(空気の温度)110度の部屋に入っても火傷しませんし、そのような気温の部屋に好んで入る人もいます(サウナ)。ケーキやクッキーをオーブンで焼く時、オーブン内の気温は170度くらいにしますが、焼けた直後の170度くらいのオーブンの中に手を入れても(温度170度の空気の中に手を入れても)端に触らなければ火傷しません。 「熱いという感覚」と「温度(温度計で測った値)」って、必ずしも対応しませんね。だから、客観的な話をする時には「熱いという感覚」ではなく「温度(=温度計で測った値)」を使います。
温度計で温度を測る方法は... 多分小学校で教わっていますね。温度計を入れてすぐは「温度計の値が変化する」ので「変化しなくなるまで」待ちます。この「温度計の値が変化しなくなる」という現象を「熱平衡(ねつへいこう)」と呼び、普通は、熱平衡になったときの温度計の値を「温度」と呼びます(なお、電子温度計などは、温度変化の法則に基づき、まだ温度変化している段階で、最終的な温度を予測して、表示しています)。「温度=温度計で測った値」ということで、ここまでは良いですね。
では次に、どのように場合に温度が変化するか、をまとめます。
例えば鍋に水を入れ、そこに焼いた石を入れると、水の温度が上がりお湯になりますね?(って「石焼き鍋」です(^^;)。この現象を昔の人は、石が持っていた「何か」が水に移動したため、水の温度が上がった、と解釈し、その移動した「何か」を「熱(heat)」と呼びました。最初は、目には見えないけど、何か「物質」のようなイメージで「熱素」とも呼ばれていました。
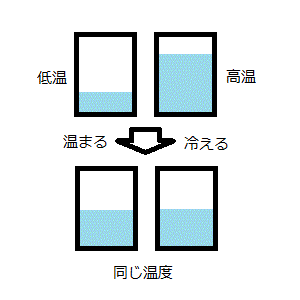
確かに熱の移動は物質(例えば水)とよく似ています。右図のように、「入れ物に水を入れた時の水面の高さ」が「温度みたいなもの」と対応します。高温のものが低温のものを温めると、その分、必ず高温の物の温度が下がります。ちょうど右の入れ物から左の入れ物に水(熱に対応)を移動させると、左の水面(温度に対応)は上がり、右の水面(温度に対応)は下がることと同じです。物には「温まりやすく冷めやすいもの」と「温まりにくく冷めにくいもの」があります。ものの「温まりにくさ」は容器の底面積に対応させると、実際の温度変化と水モデルはよく一致します。
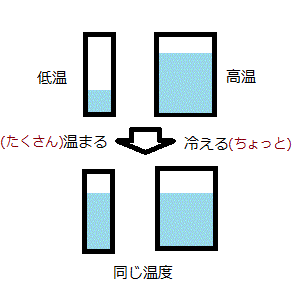
右図は、右の入れ物の方が、左の入れ物に比べが底面積がおおきくなっています。この場合、右から左に、高さが同じになるまで水を移動すると、右の入れ物の水面はあまり下がらず、左の入れ物の水面の高さは、大きく増えています。これはちょうど「熱いお湯」に「冷たい銀のスプーン」を入れると、お湯の温度はほとんど変わらずスプーンが熱くなる、という現象とおなじです。この「容器と水モデル」では、水面の高さ=温度、水=熱、底面積=熱容量(温度の上がりにくさ)に対応します。なお、温度の上がりにくさ(熱容量)は、一般に物質量に比例しますので、単位物質量当たりの温度の上がりにくさを比熱、と呼んでいます。
と、ここまでは「熱を(水のような)物質」として捉える考え方(=熱素論)で、実際の物質の温度変化を理解できますが、カルノーという人が19世紀初め「高温の物体を使わずに、低温の物体の温度が上昇することがある(水モデル=熱素論と矛盾)」ということに気が付きます。カルノーは軍人で「大砲の砲身を旋盤でけずるとき、(温める高温物体が無いのに)高温になる」という現象を見て、このことに気が付いたと言われています。が、「手をこすり合わせると手が温まる」と同じことですから、もっと早く身近な現象で気が付く人がいても良さそうに思いますが、19世紀半ばになるまで、誰もそのことに気が付きませんでした。
19世紀終わりころ「摩擦や抵抗などの、エネルギーが保存しない現象と、発熱が関係している」事にジュールという人が気が付き、「摩擦や抵抗などで失われるエネルギーと、発熱量が比例する」という実験結果を得ます。この実験事実は「摩擦や抵抗で『失われたと思っていたエネルギー』が、熱と言う形に変化した」と考えるほうが自然です。そこで「力学で導入されたエネルギーは、摩擦や抵抗など(非保存力であっても)で失われることは無く一定のままで、運動の観点から「減ったように見えるエネルギー」は、熱と言う形にへんかしただけである」と認識されるようになりました。つまり熱は(熱素という)物質ではなく、「エネルギーの一種」である、という認識です。そして「エネルギーが保存される(一定である)なら、その範囲で部分的に、水の移動のようななどイメージでも、熱移動のの現象を記述することができただけ」という位置づけで、過去の熱素論は吸収されていきます。
このような歴史を経て、「熱はエネルギーの一種であり、熱のエネルギーも含めれば、摩擦などでエネルギーが減ることは無く、保存する」という、熱の概念が形成されました。これが「熱力学の第一法則」と呼ばれる法則の中身です。
では、前節の結論を纏めていきます。
1) 熱は最初、「温度の原因」として定義された。なお「温度は温度計で測った値」であり、その意味はまだ出てきていない。
2) 熱は「温度の違う物体の間で移動する」が保存するものなので、昔は物質のようにとらえられていた。
3) 「熱はエネルギーの一種である」と捉えると、摩擦や抵抗などの現象で「発熱する」ことが(定量的に)説明できる。
まず、温度が違う物体を接触させることにより移動する移動する(変化する)熱の量を\(dQ\)と表します。物質内のエネルギーを「内部エネルギー」とよび\(U\)で表し、内部エネルギーの変化を\(dU\)と表します。「熱はエネルギーの一種」ですから、他の物体から\(dQ\)の熱をもらえば、その物体の内部エネルギーは、その分だけ増えます。他にエネルギーのやり取りが無ければ、\(dU=dQ\)と式で表せます。この式の意味は「熱はエネルギーである」です。ところで高温の物体(熱を与える源、熱源と呼びます)がなくても、摩擦など「他から仕事をすれば」エネルギーが増えます。「エネルギー」は「仕事」をする能力であり、他から仕事をされれば、エネルギーが増えます(仕事とエネルギーの関係)。ですら、外からされる仕事を「\(dW\)」と書くと、これによっても内部エネルギーが増えます。つまり、
\[dU=dQ+dW\]
となります。この式の意味は「熱はエネルギーであり、エネルギーは保存する(だから、貰った分だ増える)」です。
ここで気体のように「押せば体積が変化する物」を考えてみます。もちろん入れ物に入れないと気体は拡散していきますから、体積\(V\)の容器に入れ、容器の一部が移動でき、体積を変化させることができる仕組みだとしてみましょう(例として、シリンダーとピストン)。シリンダーの断面積を\(S\)ピストンの位置を\(x\)とすると、\(V=Sx\)です。ピストンには中に入っている気体の圧力(\(P\))とすると、ピストンには\(P S\)の力が掛かりますから、ピストンが気体を押す力\(F\)は(作用反作用の法則で)\(F=-P S\)となります。ここでピストンに極わずかの力を加えて、少し(距離\(dx\)動かしてみます。ピストンが気体に行う仕事は、\( F dx\)であり、気体の体積は\(dV= S dx\)だけ変化します。すると、\(F=- P S, dx=\frac{1}{S}dV\)なので、ピストンが気体に行う仕事は\(F dx = - P dV\)となります。「気体にが受ける仕事\(dW\)」の一部が「ピストンを押し込むことによる仕事」です。そこで、「ピストンを押し込むことによる仕事( \(-P dV\) )」と「それ以外の原因による仕事(\(dW'\) と書くことにします)」に分けて書くことにすれば、\( dW = -P dV + dW' \) となります。つまり、\[dU = dQ + dW = dQ - P dV + dW'\] となります。この式は、「外部の物体から受けた熱( \(dQ\) )と、外部から受けた仕事(\(dW\))だけ、内部エネルギーが変化する\(dU\)」そして「外部から受けた仕事(\(dW\))は、外部からの圧縮という仕事で体積が変化する分(\(-PdV\))とそれ以外の仕事(\(dW'\))に分けられる」という意味であり、「熱はエネルギーである」ことと「熱のエネルギーを考察に加えれば、エネルギーは保存する(もらった分だけ増える)」ということを意味します。
なお、この式と状態方程式を組み合わせて、積分を行うと(微小変化を足し合わせて有限な変化の式を求めると)、例えば「断熱(熱を通さない)容器内で、体積を変化させた時に、内部の温度がどう変化するか」などの結果を求めることもできます(計算などは省略します)。これを断熱変化と言いますが、断熱膨張させると温度がどう下がるか、断熱圧縮をするとどう温度が上がるか、などを求めることができ、これは特に「冷却の技術(クーラー、冷蔵庫、冷凍庫等)」と関係して応用範囲が広いです。
では次に、熱力学の第二法則を説明します。簡単に言うと「お湯で氷を温めることはできるが、氷でお湯を温めることはできない」と言うことです。
なんでそんな「当たり前のことを?」と思うかもしれませんね。実はこれが「全然当たり前じゃない!」ことに19世紀ごろから、人類は気がつき始め、現在では「この世界の謎」の1つと認識されています。実はこれが「過去と未来は何が違うのか?時間とは何か?」と言う問題と本質的に同じ問題になっていきます。
まずなんでこんなことを考えたのか、と言う歴史から簡単に。「熱はエネルギーである」ことがわかると(それを認めると)、熱の移動とは「エネルギーの移動」と捉えることができます。エネルギー保存則(=熱力学第一法則)が成り立てば、総量は変化しないわけですから、エネルギー(熱)は移動するのみ、と捉えることができます。この熱力学第一法則の範囲で「熱の移動」の法則をみた場合、「総量が変化しなければ」どのような熱の移動も起こって良いことになります。つまり「お湯から氷に熱が移動」するなら、逆に「氷からお湯に熱が移動」しても良いのでは? と言う疑問です。多分18世紀までは「それが疑問と言うことすら気がつかない自然認識であった」時代だったと思います。論理的には「氷からお湯に熱(エネルギー)が移動」しても良いにもかかわらず、実際には(つまり自然法則としては)には「氷からお湯に熱が移動する(つまり氷でお湯を温める)ことができない」。これは「当たり前」ではなく「注目すべき、自然の法則」である、と言う認識がようやく19世紀に生まれました。それが「熱力学の第2法則」です。
もう少し言い換えると、「熱は、高温物体から低温物体に移動する」同じことを逆に言えば「熱は、低温物体から高温物体に移動することは無い」、と言えます。このことを定量的に記述するために「エントロピー変化」と言う量が導入されました(エントロピーとは何か、は次回およびその次の説明になります。ここではそう言う名前の量、と思ってください)。温度\(T\)の物体が熱\(dQ\)をもらう時、その物体のエントロピー変化を\(ds= \frac{dQ}{T}\) と定義します。いくつかの物体がある時、それぞれの物体の温度\(T_i\)、それぞれの物体がもらう熱を\(dQ_i\)とし、それぞれの物体のエントロピー変化を\(ds_i= \frac{dQ_i}{T_i}\)で定義します。 その上で、それらの物体全部のエントロピー変化を\(ds=\sum_{i} ds_i=\sum_{i} \frac{dQ_i}{T_i}\) を「全エントロピー変化」と定義します。すると「高温物体から低温物体に移動する」場合には\(ds>0\)、「低温物体から高温物体に移動する」場合には\(ds<0\) となります。
つまり「熱は低温物体から高温物体に移動することはない」と言うことは、\[ ds=\sum_{i} ds_i=\sum_{i} \frac{dQ_i}{T_i} \geq 0 \] と定式化できます。これが、熱力学の第2法則です。と言っても、よくわからないですよね(^^; 詳しくは「次回」また説明します。
ついでに「熱力学の第3法則」について説明します。第2法則でエントロピー「変化」を定義しましたが、そもそもの「エントロピーと言う量」については、まだ何も定義していません(^^; それを定義するのが第3法則で、「絶対温度0度(\(T=0\))」の時、「エントロピー\(S\)は0である」と定義します。つまり、\[S(T=0)=0\]と定義します。するとそこからの「エントリピー変化」は第2法則で定義されているので、任意の状態のエントロピーが第3法則と第2法則で定義されます。
... って、結局「定義」はいろいろ出てきたけど、「それって何?」と言うイメージが、全然できませんね(^^;;
そうなんです。イメージが浮かばないけど、不思議と熱現象については、この3法則から全て導ける、と言う形にまとまっており、そのような意味で「熱力学は、芸術的(数学的)」と良い意味でも悪い意味でも言われます(^^; 式があれば計算はできるけど、何を意味しているのかイメージが全く掴めない。多分当時の(19世紀の)物理学者も同じことを感じていたと思います(^^;
最初に紹介した、熱力学の3法則の式と意味をまとめます。
1) \(dU=dQ+dW = dQ-PdV+dW' \)
熱はエネルギーであり、力学的エネルギーと熱エネルギーを加えたものは保存する。
2) \( dS= \sum_i{dS_i}=\sum_i{\frac{dQ_i}{T_i}} \geq 0 \)
熱は低温物体から高温物体へは流れない(氷でお湯を温められない)。これを「エントロピー変化」と言う量を導入して表現すると、「エントロピー変化は減少しない」と言う形にまとめられる。これを「エントロピー増大則」とも言う。
3) \(S(T=0)=0\)
絶対温度0度のエントロピーは0とする。この基準と第2法則の「エントロピー変化」を組み合わせると、任意の状態のエントロピーが定義される。----
ここまででは、特に「エントロピーって(確かに定義はされているけど)何?」と言うことがわかりませんね(^^; また、「氷でお湯を温められない」と言う、当たり前にも思えることが、何の役に立つ(知見を広げる)の? と思うかもしれませんね。そこで次回は、第2法則を認めると「熱機関(エンジン)の最大効率」を求めることができる話や「熱力学的温度計(つまり温度の定義)」を作る話が、定式化されることを紹介していきます。実は、エントロピーと言う量が考案される前に「蒸気エンジンの効率を上げるにはどうしたら良いか(同じ燃料でたくさんの仕事ができるエンジンはどう作れば良いか?)」と言う、極めて現実的な(儲け話にも繋がる)問題に対する研究から、様々な計算が行われました。その後、その様々な計算結果の解釈などを通して、最終的に「エントロピー」と言う概念が発見されました。その道筋は、結構長くとても面倒になりますので、この授業では逆に「エントロピー増大則(熱力学第2法則)」を認めたら、そこからどのような結論が得られるか? と言う順番で、簡潔に整理して、紹介します。最終的に「物質によらない(何で作っても)一位的に温度目盛りが決まる『熱力学的温度計』が定義できること」を示し、現在(国際標準単位SIで)使われている「温度」の意味を、まとめていきます。
それでも「エントロピーって何もの?」と言う疑問が残ると思いますが、それはその次の「分子運動による熱現象の解釈」の話で紹介していきます。その段階で熱現象も「古典物理学の基本法則」と関連づきますので、本授業の話の「本筋」はそこからです。それまでは、多少ピンとこないことがあっても「前置き」と思ってください。
では、今日は、このへんで終わります。